La production d’hydrogène constitue un enjeu majeur pour l’avenir de la filière hydrogène. Utiliser des ressources renouvelables est de plus un impératif pour s’inscrire dans une démarche de développement durable. Pour cela, on peut s’inspirer des processus chimiques à l’œuvre naturellement dans certains micro-organismes photosynthétiques tels que les algues vertes et les cyanobactéries, qui ont la particularité de produire de l’hydrogène à partir de l’eau, sous l’effet de la lumière.
Actuellement, tous les dispositifs technologiques développés pour produire ou utiliser l’hydrogène renferment des métaux nobles
[1] tels que le platine comme catalyseurs. Les analyses montrent aujourd’hui que les réserves en platine sont limitées et que la rareté et le coût de ce métal ne permettent pas d’envisager une économie basée sur l’hydrogène sur le long terme, malgré les efforts pour en diminuer les quantités dans les électrolyseurs et les piles. C’est là qu’une démarche biomimétique permet de s’affranchir du recours au platine, en permettant la préparation de catalyseurs à base de métaux plus abondants et moins chers qui sont utilisés par les organismes naturels (fer, nickel, cobalt, manganèse).
Pour reproduire et améliorer les processus biologiques de photoproduction d’hydrogène, le chimiste cherche à élaborer des systèmes complexes renfermant un photosensibilisateur, capable de capter l’énergie lumineuse et d’induire une séparation de charge, et un catalyseur qui utilise l’électron ainsi photogénéré pour réduire l’eau en hydrogène.
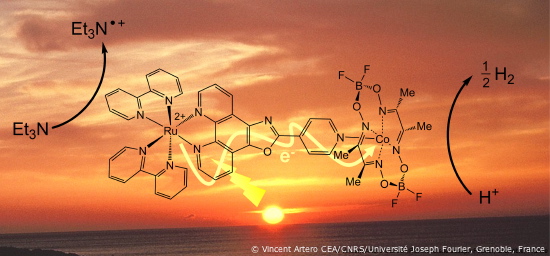
Une première version d’un tel ensemble a été mise au point avec des systèmes supramoléculaires, c’est-à-dire où une même molécule assure plusieurs fonctions, comportant un photosensibilisateur et un catalyseur à base de cobalt. Sous l’effet de la lumière, les électrons fournis par donneur sacrificiel (la triéthylamine) sont utilisés pour la réduction de l’eau en hydrogène catalysée au niveau de l’atome de cobalt, avec une efficacité supérieure aux systèmes comparables à base de métaux nobles (Pd, Rh et Pt) précédemment décrits. Certes, le système utilise encore le ruthénium pour ses propriétés photochimiques. Une prochaine étape visera à s’en affranchir.
Même si, à la façon des organismes vivants, l’utilisation de l’eau non seulement comme source de protons, mais aussi comme source d’électrons (évitant ainsi d’avoir à ajouter une molécule organique) reste l’objectif ultime de ces recherches, ce résultat constitue une avancée considérable dans le domaine de la photo-production d’hydrogène.
[1] Historiquement, les métaux nobles étaient les métaux précieux (or, argent, platine) utilisés en orfèvrerie. Cela correspond pour le chimiste à des métaux qui ne s’oxydent pas facilement. Ce terme s’applique maintenant aux autres métaux qui présentent une faible abondance dans la croûte terrestre et sont donc à la fois rares et coûteux (palladium, rhodium, iridium).