La recherche de sources d'énergie propres représente un objectif prioritaire pour nos sociétés modernes aux besoins en énergie croissants. La mise au point de procédés de production d’hydrogène via des ressources renouvelables telle que l’eau et, par exemple, l’énergie solaire représente une solution séduisante. Les coûts de production d’hydrogène restent cependant élevés à cause notamment de l’utilisation du platine, très peu abondant, comme catalyseur dans les systèmes d’électrolyse à membrane. Trouver de nouveaux catalyseurs dont le coût et la disponibilité permettent un développement industriel à grande échelle constitue donc un enjeu majeur. Or, dans la nature, les hydrogénases [NiFe] sont capables de catalyser la production du dihydrogène avec une grande efficacité et en conditions douces, tout en utilisant des métaux aussi abondants que le nickel ou le fer.
En reproduisant au sein d’une molécule de synthèse les éléments clefs du site actif de ces enzymes, il devient alors possible,
via une démarche dite bio-inspirée, de développer de nouveaux catalyseurs sans métaux nobles. Cependant, les modèles biomimétiques nickel-fer décrits jusqu’à maintenant ne reproduisent pas la réactivité centrée sur l’ion nickel du site actif de ces enzymes et affichent ainsi des performances modestes.
C’est dans ce contexte que des chercheurs de notre laboratoire, en collaboration avec une équipe du Département de Chimie Moléculaire et dans le cadre du Labex ARCANE [
Collaboration], ont développé un modèle structural et fonctionnel qui relocalise la réactivité sur le centre nickel, grâce à l’utilisation d’un ligand bipyridine-dithiolate. Ceci est attesté par la détection de deux intermédiaires impliqués dans le cycle catalytique de production d’hydrogène qui reproduisent les caractéristiques structurales et électroniques de deux états (Ni-L et Ni-R) du cycle enzymatique.
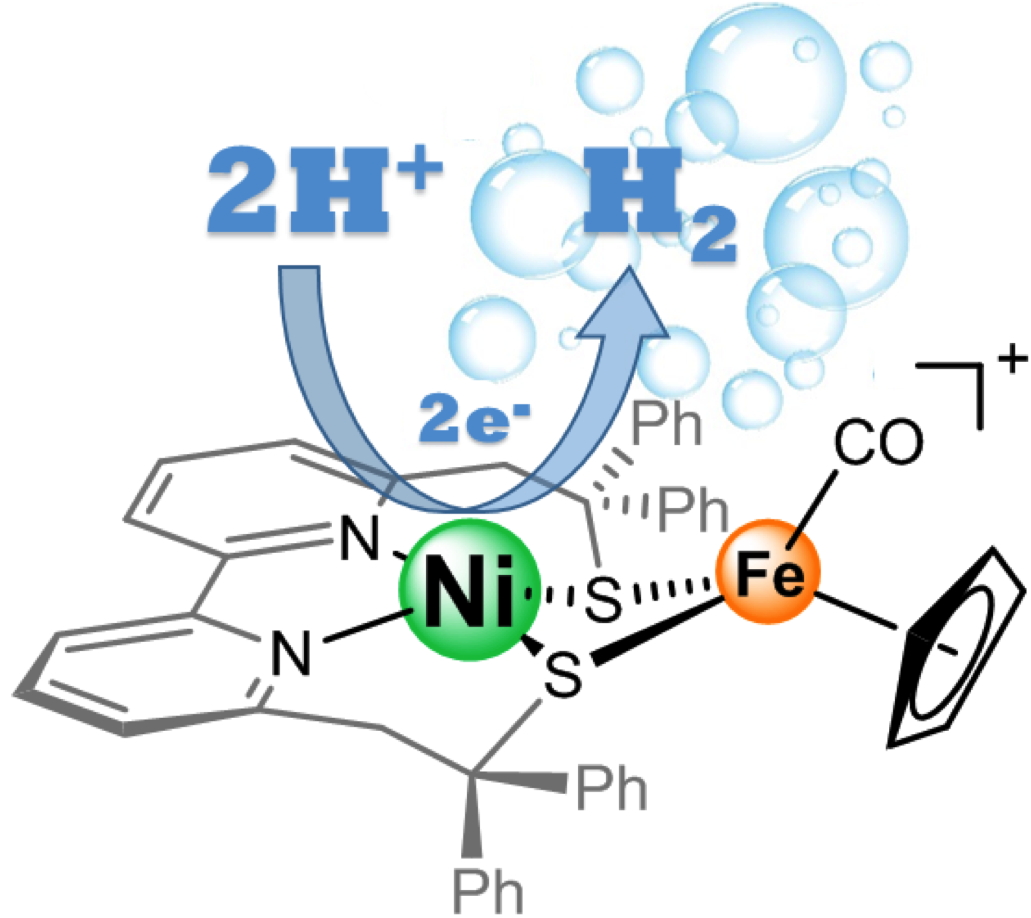
Premier modèle dont l’activité catalytique est centrée sur le nickel de l’hydrogénase [NiFe].
La vitesse de production d’hydrogène catalysée par ce composé original montre sans ambiguïté la mise en synergie des ions nickel et fer pour la production d’hydrogène. En effet, le complexe mononucléaire de nickel est 10 fois moins actif et le complexe mononucléaire de fer ne présente pas d’activité. Une évaluation comparée des performances du nouveau catalyseur nickel-fer révèle que celles-ci surpassent largement celles des autres modèles biomimétiques dinucléaires.
Ce travail ouvre de nouvelles perspectives dans le développement de structures mimant de façon efficace l’activité des hydrogénases [NiFe].
Collaboration : Département de Chimie Moléculaire de l’Université Grenoble Alpes ; Université de Göttingen, Allemagne ; iSm2, Université Aix Marseille ; Inac-SyMMES, CEA-Grenoble.
Ces travaux de recherche ont a été financés par le labex ARCANE.