Une métalloenzyme artificielle (ArM) est une construction hybride résultant de la combinaison d'un complexe synthétique inorganique et d’une macromolécule biologique (ADN ou protéine). L'ensemble forme un catalyseur éco-compatible qui fonctionne dans des conditions douces conformément aux principes de la chimie verte. Toutefois, il serait intéressant d'améliorer les propriétés de ces ArM dans le but d'élargir leur gamme de substrats (limitée notamment par la solubilité en phase aqueuse), d'augmenter le nombre de cycles catalytiques (limité par la stabilité des protéines dans le milieu oxydant) et d’élargir la diversité des réactions catalysées (accéder à des combinaisons de processus catalytiques). Une étape importante pour aller dans ce sens a été franchie en proposant ces catalyseurs sous une forme solide afin de réaliser une catalyse hétérogène (liquide-solide).
C’est dans ce contexte que des chercheurs de notre laboraoire conçoivent des ArM afin de proposer de nouvelles méthodes de catalyse durable pour les réactions d’oxydation. Ils ont ainsi développé plusieurs systèmes remarquables basés notamment sur la protéine NikA à laquelle divers complexes synthétiques inorganiques de fer, de manganèse ou de ruthénium ont été ancrés. Cette enzyme, responsable du transport du nickel chez les bactéries, peut servir de support aux catalyseurs inorganiques conçus par les chercheurs. Ces derniers ont ainsi mis au point une version originale d’une ArM dans laquelle des cristaux de NikA ont été stabilisés par réticulation par la technique « Cross-Linked Enzyme Crystals » ou CLEC. Cette technologie permet d’améliorer la stabilité et le nombre de recyclages des catalyseurs tout en rendant possible l'élargissement des conditions réactionnelles utilisées (solvants, pH, températures).
Après avoir défini les conditions de réticulation des cristaux d’ArM et s’être assuré qu’ils étaient stables dans des mélanges eau-solvant organique (de 4 à 70 °C et en présence d'oxydants), leurs propriétés catalytiques ont pu être évaluées. Les chercheurs ont ainsi montré que ces catalyseurs hétérogènes présentent une meilleure efficacité que leurs homologues solubles en ce qui concerne la sulfoxydation des dérivés du thioglycolamide. En effet, les produits de cette réaction d’oxydation ont pu être obtenus avec une efficacité multipliée par 8 et en présence de très faibles quantités de catalyseur (0,1 %). De plus, même limité à quatre, le nombre de recyclages montre que ces systèmes sont efficaces dans des conditions dures puisque l’oxydant utilisé, l'hypochlorite de sodium, est très agressif.
La grande originalité de ce catalyseur hybride solide est de permettre la stabilisation du site catalytique artificiel au sein du cristal de protéine, ceci en travaillant en milieu aqueux, en présence de faibles quantités de catalyseur, lui-même étant recyclé. La conception d'enzymes artificielles cristallines représente ainsi une alternative prometteuse aux enzymes solubles ou aux enzymes supportées pour l'avenir de la biologie synthétique.
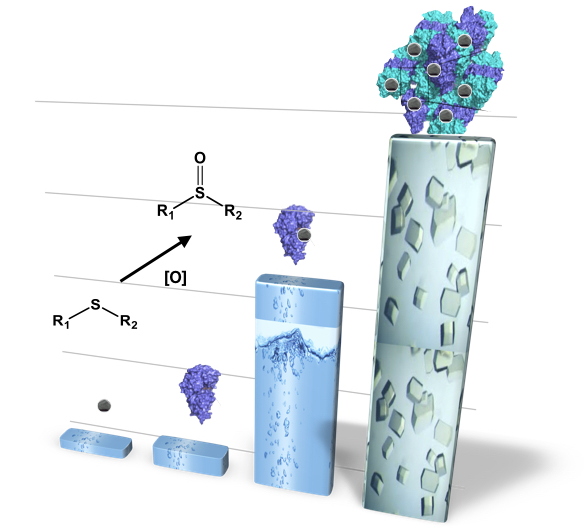 Un cristal CLEC-ArM est constitué d'hybrides NikA-FeL3 (FeL3 étant un complexe de fer avec un ligand coordinant le fer par deux atomes amines et deux pyridines) réticulés avec du glutaraldéhyde. La stabilité des cristaux dans un mélange de solvants eau-acétonitrile-1-1 permet d'utiliser de nombreux substrats lipophiles et de tester différentes réactions d'oxydation, ici la sulfoxydation.
Un cristal CLEC-ArM est constitué d'hybrides NikA-FeL3 (FeL3 étant un complexe de fer avec un ligand coordinant le fer par deux atomes amines et deux pyridines) réticulés avec du glutaraldéhyde. La stabilité des cristaux dans un mélange de solvants eau-acétonitrile-1-1 permet d'utiliser de nombreux substrats lipophiles et de tester différentes réactions d'oxydation, ici la sulfoxydation.
Ce travail réunit à la fois, la synthèse, la catalyse et l'étude cristallographique des protéines. Il résulte d'une collaboration entre deux équipes du laboratoire Chimie et Biologie des Métaux : l'équipe Chimie Bioinspirée et Environnement et l'équipe BioCatalyse.
Ce travail a été financé par l'ANR CrystalBall (financement d’un CDD et d’un post-doc) et par le Labex ARCANE qui a financé la thèse du Dr Sarah Lopez.