Les réactions de transfert multiélectroniques et multiprotoniques sont au cœur de processus biologiques et chimiques essentiels tels que l'activation de petites molécules et la conversion d'énergie. L'optimisation de la cinétique de ces réactions est un défi majeur pour les applications liées à l'énergie. La nature utilise largement les métaux de la première série de transition dans les processus enzymatiques pour catalyser ces réactions dans des conditions particulièrement douces. Nous nous inspirons de ces systèmes (approche bio-inspirée) pour concevoir des plateformes catalytiques innovantes pour la production d’hydrogène, la valorisation du dioxyde de carbone et la fixation de l’azote.
Nous exploitons ensuite ces plateformes catalytiques en les intégrant dans des électrodes à base de nanotubes de carbone (
axe II) ou en les assemblant avec diverses unités photo-actives pour obtenir des assemblages photo-électrocatalytiques fonctionnels
(axe III).
 Hydrogène
Hydrogène
La production et la dissociation de l’hydrogène (H
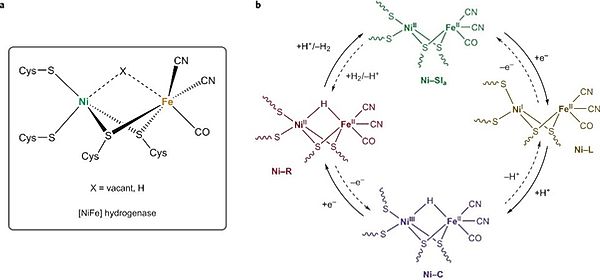
2) sont deux réactions catalysées par les hydrogénases au sein de sites dinucléaires de type NiFe et FeFe. En se basant sur les connaissances toujours plus fines de ces systèmes biologiques, notre équipe développe de nouveaux catalyseurs bio-inspirés et biomimétiques pour la production d’hydrogène.
La conception de catalyseurs biomimétiques pour la production d’hydrogène est au cœur de l'expertise de l'équipe SolHyCat. Depuis 2006, notre groupe a étudié de nouveaux catalyseurs reproduisant les principales caractéristiques structurales, spectroscopiques et de réactivité du site actif des hydrogénases [NiFe].
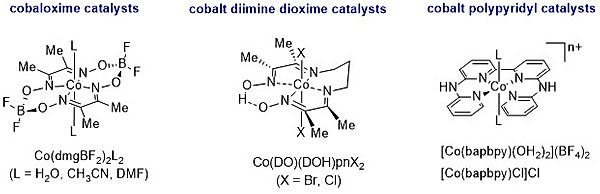
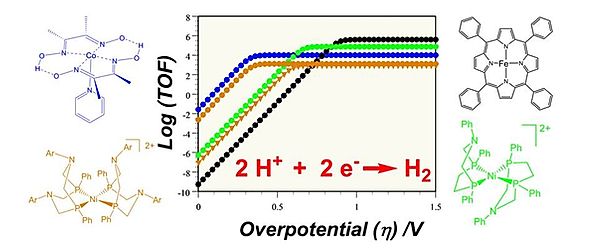
En parallèle, un large pan de nos activités concerne l’étude de complexes de cobalt catalysant cette réaction. Cette étude comprend les cobaloximes et les complexes diimine-dioxime de cobalt ainsi que de nouvelles plateformes catalytiques développés plus récemment telles que les complexes [Co(bapbpy]
2+. Pour tous ces systèmes moléculaires, nous appliquons les méthodes analytiques les plus récentes pour déterminer leur mécanisme catalytique, identifier le rôle des groupements redox-actifs et des relais de protons (pont oxime, groupes amine pendants...) qu’ils contiennent et pour comparer leur activité catalytique avec celle d'autres catalyseurs moléculaires de la littérature.
 Valorisation du CO2 et fixation de l’azote
Valorisation du CO2 et fixation de l’azote
Les sites actifs des CO-déshydrogénases et des formiate-déshydrogénases contiennent des sites basiques à proximité des sites métalliques où le CO
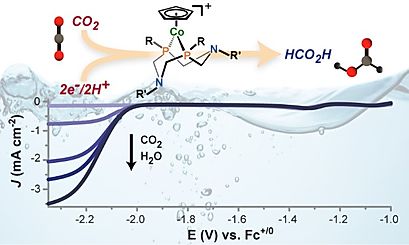
2 est activé. Ici-encore, nous pouvons donc appliquer des concepts de bio-inspiration pour concevoir de nouvelles plateformes catalytiques moléculaires plus efficaces pour la conversion du CO
2. Dans cette perspective, les complexes de cobalt de structure [CpCoP2N2] (figure) s'avèrent très prometteurs.
Notre intérêt pour les réactions de transfert multiélectroniques et multiprotoniques complexes nous a naturellement amenés à nous interroger sur les bases fondamentales permettant la réaction de réduction de l’azote moléculaire (N
2) par les organismes diazotrophes. Cela nous conduit, à développer des plateformes organiques multivalentes capables de stabiliser des clusters de sulfure métalliques, dont la composition s’approche des cofacteurs naturels des nitrogénases. Une étude systématique de la réactivité de nos assemblages synthétiques sur différents substrats de cette enzyme nous aidera à déchiffrer les paramètres critiques régissant l'activité de ces biomolécules.