 Projet scientifique
Projet scientifique
Dans le cadre de la biologie de synthèse, la biocatalyse représente la solution la plus prometteuse pour développer une chimie durable. Pourtant, il reste notamment à développer les réactions abiotiques et la stabilité des biocatalyseurs.
L'approche que nous développons consiste en la mise au point de métalloenzymes artificielles (ArMs) : des complexes inorganiques bio-inspirés sont introduits au sein de cavités hydrophobes de protéines. Le complexe inorganique joue le rôle du centre réactif alors que la protéine apporte stabilité et (énantio)sélectivité. L'objectif de notre projet est de mettre au point des catalyseurs hybrides actifs dans le cadre d'oxydations en privilégiant les réactions de transfert d'oxygène asymétrique sur une quantité non limitée de substrat.
 Catalyseurs chiraux hybrides protéiques : vers des métalloenzymes artificielles hétérogènes et multifonctionnelles
En collaboration avec le GMTC et C. Cavazza de l'équipe BioCat de notre laboratoire.
Catalyseurs chiraux hybrides protéiques : vers des métalloenzymes artificielles hétérogènes et multifonctionnelles
En collaboration avec le GMTC et C. Cavazza de l'équipe BioCat de notre laboratoire.
Malgré tous les progrès faits en recherches, il est difficile, aujourd'hui encore, de prévoir le résultat d'une catalyse chimique énantiosélective. Une approche combinatoire récente, pour la sélection de catalyseurs énantiosélectifs efficaces, a montré que plusieurs paramètres extérieurs (le solvant ou le contre-ion), en dehors de la structure du ligand chiral, avaient une influence inattendue sur l'énantiosélectivité de la réaction. Leur influence est cependant totalement prise en charge dans le cas des métalloenzymes naturelles, la première ainsi que la deuxième sphère de coordination du métal sont fixées et sont le résultat de l’évolution au cours des âges.
Globalement, les approches chimiques et biochimiques sont complémentaires. Un catalyseur hybride comprenant une partie protéique et un complexe métallique représente donc une bonne solution catalytique. Quand ce catalyseur peut, en plus, être hétérogénéisé, il représente alors le catalyseur idéal.
L'objectif de notre projet est de mettre au point des catalyseurs hybrides hétérogènes actifs dans le cadre d'oxydations - en privilégiant les réactions de transferts d'oxygène asymétriques – mais aussi multifonctionnels, c’est-à-dire capables de réaliser une cascade réactionnelle. L'avantage de cette méthode est que l'optimisation de ces catalyseurs se fera à la fois par mutagenèse dirigée et par « mutagenèse chimique » (la structure du catalyseur inorganique pouvant être modifiée). Nous avons commencé par privilégier des interactions non covalentes entre les deux partenaires de l'hybride. Afin de donner plusieurs fonctions à un même objet, nous ajoutons maintenant un deuxième site catalytique par liaison covalente.
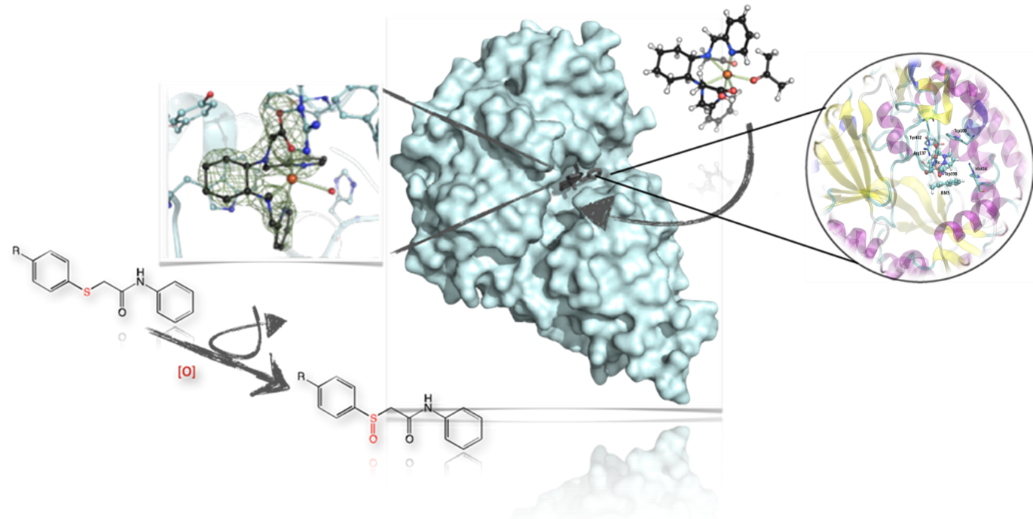
L’un des premiers résultats de l’équipe dans ce domaine fut l'introduction de complexes de type Fe-N2Py2 modifiés dans la protéine NikA, une protéine de transport du nickel chez
E. coli. Nous avons pu alors démontrer qu'il existe une synergie entre les deux partenaires de l'hybride car nous observons une sélectivité de la réaction d'oxydation, ici un transfert d'oxo sur un thioéther, seulement dans le cas de l'hybride grâce à la sélection du substrat le plus affin pour cette ArM par des calculs de docking. [Esmieu
et al.
Ang. Chem. Int. Ed.,
2013]
Il est aussi possible de travailler avec des métaux non naturels comme le ruthénium. L’hydrochloration d’alcènes par un iode hypervalent est catalysée seulement lorsque le complexe est inséré dans la cavité de la protéine, provoquée par la perte d’un ligand ouvrant une position labile essentielle à l’activation de l’oxydant. [Lopez
et al.
Chem. Commun., 2017]
Si ces ArMs offrent conceptuellement des perspectives énormes pour la chimie verte, il faut encore relever un défi technologique pour développer par ingénierie des enzymes efficaces pour la production de chaque molécule d'intérêt. Pour cela, il faut trouver le meilleur couple protéine/catalyseur, comprendre son fonctionnement, et l'adapter… Dans ce but, une avancée majeure fut le développement d’une méthode qui permet de suivre la réaction chimique au niveau du site actif au cours du temps au sein même d’un cristal de protéine. Cette méthode nous offre ainsi une vision en direct de la réaction du catalyseur avec son substrat et devrait permettre de définir, à l'avenir, les déterminants structuraux du contrôle énantiosélectif de l’ArM. En collaboration avec C. Cavazza de notre laboratoire, équipe BioCat, nous avons suivi,
in cristallo, étape par étape, une hydroxylation aromatique catalysée par un complexe inorganique de fer au sein de la protéine NikA. L’état cristallin permet la diffusion des substrats et des intermédiaires de la réaction. L'enzyme reste active ; la réaction peut se faire et il est possible d'en suivre les différentes étapes. [Cavazza
et al.
Nature Chemistry,
2010]
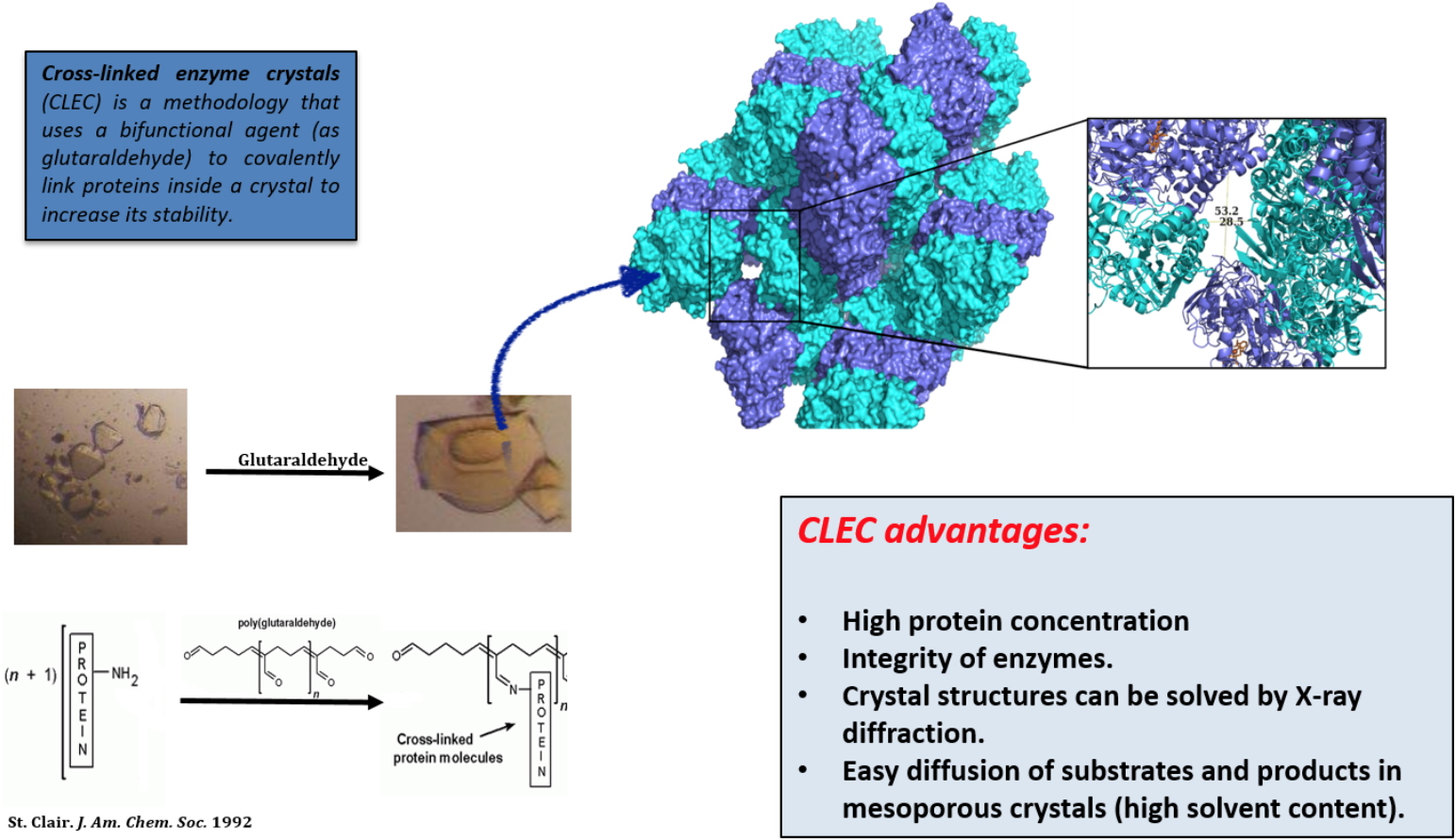
Cette méthode a été le point de départ du projet de réactivité
in cristallo. Nous avons mis au point des catalyseurs hybrides hétérogènes grâce à une stabilisation des cristaux protéiques par la technique CLEC (Cross Linked Enzyme Crystals). Dans ces CLEC, sont internalisés, au choix, nos complexes de fer en fonction de la réaction visée. Ces catalyseurs hétérogènes sont très stables vis-à-vis des conditions oxydantes, solvants organiques, agitation, température, pH. Ils nous ont permis de réaliser, par exemple, une réaction de coupure oxydante d’alcènes en utilisant le dioxygène de l’air avec un TON supérieur à 30 000 [Lopez
et al.
J. Am. Chem. Soc.,
2017].
Nous aimerions maintenant développer le concept de catalyse en cascade in cristallo sur les transformations oxydantes d’alcènes, réalisées dans des cristaux d’ArMs réticulées (
CLEC-ArM) à sites actifs multiples. Il s'agira d'une évolution de notre application CLEC maintenant maîtrisée mais qui nécessite des modifications chimiques innovantes sur les cristaux de protéine eux-mêmes pour l'insertion covalente d'un second site catalytique inorganique. Nos connaissances en matière de haute performance de la dégradation des alcènes en utilisant le dioxygène comme oxydant nous conduiront à ajouter des transformations en aval dans une cascade originale de réactions d'oxydations catalytiques, impliquant la carbonatation, l'oxydation d'aldéhydes ou la dégradation de biomolécules polyinsaturées.
Une version photocatalytique est aussi envisagée en greffant des photosensibilisateurs (des complexes de ruthénium par exemple) en plus d’un site catalytique au sein de
cristaux de la protéine LEAFY.
Enfin, nous explorons également la possibilité d’utiliser un autre type de biomolécules, les G-quadruplex, comme support des catalyseurs inorganiques [ANR CoolCat 2018].

 Publications
Lopez S, Mayes DM, Crouzy S, Cavazza C, Leprêtre C, Moreau Y, Burzlaff N, Marchi-Delapierre C and Ménage S
Publications
Lopez S, Mayes DM, Crouzy S, Cavazza C, Leprêtre C, Moreau Y, Burzlaff N, Marchi-Delapierre C and Ménage S
A Mechanistic Rationale Approach Revealed the Unexpected Chemoselectivity of an Artificial Ru-dependent Oxidase - A Dual Experimental/Theoretical Approach
ACS Catalysis, 2020,
10(10): 5631–5645.
Cavazza C, Marchi-Delapierre C and Ménage S
Chapter 7: Hybrid catalysts for oxidation reactions Book chapter in Artificial Metalloenzymes and MetalloDNAzymes in Catalysis, 2017.
Lopez S, Rondot L, Cavazza C, Iannello M, Boeri-Erba E, Burzlaff N, Strinitz F, Jorge-Robin A, Marchi-Delapierre C and Ménage S
Efficient conversion of alkenes to chlorohydrins by a Ru-based artificial enzyme.
Chemical Communications, 2017,
53(25): 3579-3582
Lopez S, Rondot L, Leprêtre C, Marchi-Delapierre C, Ménage S and Cavazza C Cross-linked artificial enzyme crystals as heterogeneous catalysts for oxidation reactions.
Journal of the American Chemical Society, 2017,
139(49): 17994-18002
Rondot L, Girgenti E, Oddon F, Marchi-Delapierre C, Jorge-Robin A and Ménage S Catalysis without a headache: Modification of ibuprofen for the design of artificial metalloenzyme for sulfide oxidation.
Journal of Molecular Catalysis A: Chemical, 2016,
416: 20-28
Marchi-Delapierre C, Rondot L, Cavazza C and Ménage S Oxidation catalysis by rationally designed artificial metalloenzymes.
Israel Journal of Chemistry, 2015,
55(1): 61-75
Esmieu C, Cherrier MV, Amara P, Girgenti E, Marchi-Delapierre C, Oddon F, Iannello M, Jorge-Robin A, Cavazza C and Ménage S Oxygenase built from scratch: Substrate binding site identified using a docking approach.
Angewandte Chemie International Edition, 2013,
52(14): 3922-3925
Cherrier MV, Girgenti E, Amara P, Iannello M, Marchi-Delapierre C, Fontecilla-Camps JC, Ménage S and Cavazza C The structure of the periplasmic nickel-binding protein NikA provides insights for artificial metalloenzyme design.
Journal of Biological Inorganic Chemistry, 2012,
17(5): 817-829
Oddon F, Girgenti E, Lebrun C, Marchi-Delapierre C, Pécaut J and Ménage S Iron coordination chemistry of N
2Py
2 ligands substituted by carboxylic moieties and their impact on alkene oxidation catalysis.
European Journal of Inorganic Chemistry, 2012,
2012(1): 85–96
Cavazza C, Bochot C, Rousselot-Pailley P, Carpentier P, Cherrier MV, Martin L, Marchi-Delapierre C, Fontecilla-Camps JC and Menage S Crystallographic snapshots of the reaction of aromatic C-H with O
2 catalysed by a protein-bound iron complex.
Nature Chemistry, 2010,
2(12): 1069-1076
Rousselot-Pailley P, Bochot C, Marchi-Delapierre C, Jorge-Robin A, Martin L, Fontecilla-Camps JC, Cavazza C and Ménage S The protein environment drives selectivity for sulfide oxidation by an artificial metalloenzyme.
Chembiochem, 2009,
10(3): 545-552