Le cuivre est par ses propriétés d'oxydo-réduction (Cu(I)/Cu(II)) un élément à la fois essentiel à la vie et toxique, dont l’homéostasie est maintenue par de multiples mécanismes. Dans l’organisme, l’excrétion du cuivre excédentaire se produit dans le foie qui le rejette vers la bile. Certaines maladies proviennent de dysfonctionnements de protéines de transport qui assurent l’homéostasie du cuivre et conduisent à l’accumulation de celui-ci dans les hépatocytes, provoquant cirrhose et destruction progressive du foie. Le relargage du cuivre accumulé induit à son tour des troubles neurologiques. Ces maladies sont incurables et rapidement fatales en absence de traitement. La diversité des effets de ces intoxications par le cuivre est telle que les maladies sont difficiles à diagnostiquer et les traitements souvent tardifs. Parmi les toxicoses à cuivre, la maladie de Wilson, la mieux caractérisée, provient de mutations du gène ATP7B qui rendent défectueuse l’excrétion du cuivre vers la bile.
Les traitements actuels visent à limiter l’absorption de cuivre dans l’organisme par ingestion de chélateurs du cuivre agissant dans le plasma pour limiter son entrée dans l’organisme (pénicillamine, trientine) ou de zinc stimulant la synthèse des métallo-thionéines pour arrêter le cuivre dans les enthérocytes. Ces chélateurs, peu spécifiques du cuivre, ont beaucoup d’effets secondaires ; lorsqu’ils ne sont pas efficaces, la seule solution est la transplantation hépatique.
La mise au point de nouveaux chélateurs visant spécifiquement le cuivre dans les hépatocytes est issue d’une collaboration entre des chercheurs de notre laboratoire et l’équipe Reconnaissance Ionique du Service de Chimie Inorganique et Biologique de l'Inac concernant la chélation des métaux dans le vivant (programme de toxicologie nucléaire du CEA). L’étude des caractéristiques fondamentales de la coordination du Cu(I) par des peptides et des protéines a amené les chimistes au design de molécules dédiées à la chélation spécifique du Cu(I) en milieu intracellulaire. En collaboration avec l'Inserm UMR 757, l'équipe Biologie des Métaux du laboratoire Chimie et Biologie des Métaux a entrepris de mesurer un signal intracellulaire traduisant l’élévation de la concentration de cuivre dans des hépatocytes en culture. Ces chercheurs ont ainsi démontré que le chélateur P3, dont la synthèse a été réalisée en collaboration avec le Département de Chimie Moléculaire de l'UJF, est capable de ramener le cuivre intracellulaire à son niveau basal (Figure 1).
Le milieu de culture ne contient que le cuivre basal. La protéine est détectée dans le Golgi, entre les noyaux et le canalicule, où elle joue son rôle basal de transfert du cuivre.
Ajout de 1 µM de CuSO4 au milieu de culture pendant 2 heures. La protéine encercle les canalicules et joue son rôle de détoxication en transférant le cuivre dans le canalicule.
Ajout de 1 µM de CuSO4 au milieu de culture pendant 2 heures, puis de 10 µM de P3 pendant 3 heures. La protéine est à nouveau entre les noyaux et le canalicule. Le cuivre est donc retourné à son état basal grâce à P3.
P
3 est le chef de file d’une nouvelle famille de chélateurs conçus pour (i) être spécifiques du Cu(I) pour ne pas troubler l’homéostasie du Zn(II) (rapport d’affinités de 10
10) ; (ii) cibler les hépatocytes (P3 entre dans différentes lignées cellulaires) ; (iii) s’activer dans le cytoplasme (P3 ne fixe pas le cuivre en absence de réducteur) (
Figure 2).
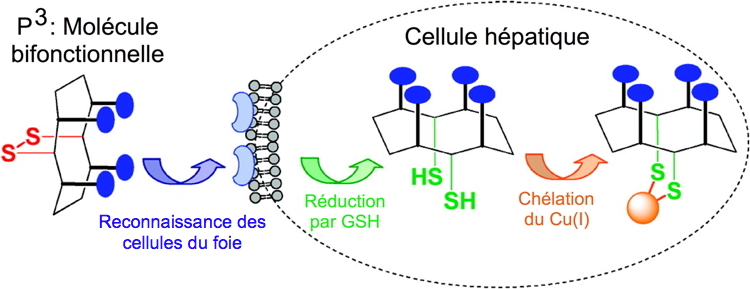
Figure 2 : P3, première molécule remplissant les conditions (i) à (iii).
Les résultats obtenus pour P
3 permettent d’envisager maintenant ces molécules comme de potentiels médicaments pour lutter contre les intoxications du foie par le cuivre et ainsi participer à une nouvelle approche thérapeutique.
L’homéostasie est l’équilibre dynamique qui nous maintient en vie. L'homéostasie est la maintenance de l'ensemble des paramètres physico-chimiques de l'organisme qui doivent rester stables (glycémie, température, taux de sel dans le sang, etc.).